Publié par Guy Jovelin le 28 juillet 2021
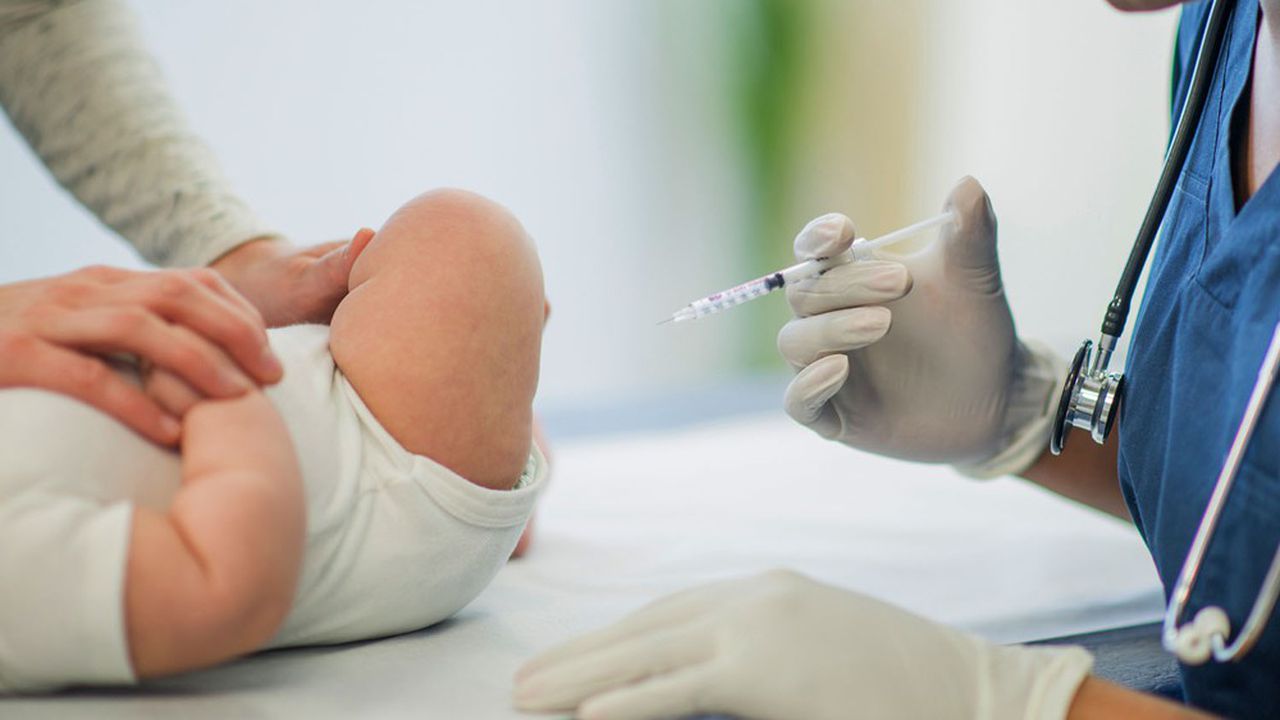
Pfizer et Moderna élargissent la taille de leurs essais cliniques sur les injonctions expérimentales covid-19 car l’objectif est également de vacciner les enfants âgés de cinq à onze ans, voire plus jeunes encore. La sollicitation est venue directement de la Food and Drug Administration des Etats-Unis (FDA).
Comme le rapporte le New York Times, les deux fabricants de vaccins élargissent la taille de leurs essais cliniques par mesure de précaution conçue pour détecter des effets secondaires rares disent-ils, notamment des problèmes d’inflammation cardiaque, survenus chez des personnes vaccinées de moins de 30 ans. Mais d’ores et déjà, lors d’une réunion en Ohio, le président Joe Biden a promis que l’autorisation d’urgence pour les vaccins pédiatriques arriverait « bientôt », mais la Maison Blanche n’a pas précisé le calendrier. Il n’est pas clair si l’élargissement des études affectera le moment où les vaccins pourraient être autorisés pour les enfants. La Food and Drug Administration a indiqué à Pfizer-BioNTech et Moderna que la taille et la portée de leurs études pédiatriques, comme initialement prévu, étaient insuffisantes pour détecter des effets secondaires rares : ceux-ci incluent la myocardite, l’inflammation du muscle cardiaque et la péricardite, l’inflammation du revêtement autour du cœur.
La FDA a demandé aux entreprises d’inclure 3 000 enfants dans le groupe des 5 à 11 ans – l’une des sources du NY Times a décrit ce chiffre comme le double du nombre initial de participants à l’étude. Un porte-parole de Moderna, Ray Jordan, a confirmé que la société avait l’intention d’étendre son essai « pour enregistrer une base de données de sécurité plus grande qui augmente la probabilité de détecter des événements plus rares. L’étude Moderna a commencé à recruter des patients dès mars dans le but d’inscrire 6 795 participants de moins de 12 ans. Les participants devaient être répartis également en trois groupes d’âge, comprenant un groupe d’âge de 6 à 11 ans de 2 265 participants chacun. Pfizer fonctionnerait plus vite que Moderna et pourrait être en mesure de répondre aux attentes de la FDA, fin septembre.
L’examen de toutes les données d’innocuité et d’efficacité prendra probablement au moins quelques semaines aux autorités de réglementation.
Pfizer avait précédemment déclaré s’attendre à des résultats pour le groupe des 5 à 11 ans en septembre et à de nouvelles preuves pour les enfants plus jeunes, âgés de 2 à 5 ans, peu de temps après. En effet, des réponses de la tranche d’âge allant de 6 mois à 2 ans sont attendues pour octobre ou novembre. Un porte-parole a déclaré lundi que la société n’avait aucune mise à jour sur son calendrier. Les questions sur la vaccination des enfants, y compris ceux de moins de 12 ans, intéressent énormément les parents et les enseignants. Les régulateurs seront tenus d’équilibrer les effets secondaires potentiels de la vaccination contre les coronavirus et les risques de Covid-19.
L’objectif étant de vacciner au plus vite également les enfants et les nourrissons, Moderna, et Pfizer a la même optique, prévoit de demander une autorisation d’urgence plus tard cette année ou au début de l’année prochaine. C’est-à-dire une autorisation qui fait fi du recul de quelques années nécessaire pour connaître les effets secondaires à moyen et long termes.
Toutes les générations doivent recevoir le sérum « miracle » contre le covid, telle est l’injonction des politiciens, organismes internationaux, gouvernements, laboratoires pharmaceutiques, médecins de plateaux… Pas de répit même pour les enfants.
Francesca de Villasmundo
Source : medias-presse.info